Elektronegativitas merupakan suatu konsep dalam kimia yang menggambarkan kemampuan suatu unsur kimia untuk menarik pasangan elektron dalam suatu ikatan kimia.
Konsep ini pertama kali diperkenalkan oleh Linus Pauling, seorang ilmuwan dan kimiawan terkemuka, yang memperkenalkan skala elektronegativitas pada tahun 1932.
Pengertian Elektronegativitas Menurut Para Ahli
Berikut ini adalah pengertian elektronegativitas menurut beberapa ahli:
1. Linus Pauling
Linus Pauling mendefinisikan elektronegativitas sebagai kemampuan suatu atom dalam suatu senyawa kimia untuk menarik pasangan elektron.
Dalam penelitiannya, ia mengusulkan bahwa skala relatif elektronegativitas dapat digunakan untuk memprediksi jenis ikatan yang akan terbentuk antara unsur-unsur tersebut.
2. Robert Mulliken
Robert Mulliken, seorang kimiawan dan fisikawan Amerika, juga memberikan kontribusi penting terhadap konsep elektronegativitas.
Menurut Mulliken, elektronegativitas dapat diinterpretasikan sebagai kecenderungan suatu atom untuk menarik elektron.
Dia menekankan bahwa elektronegativitas dapat digunakan untuk memahami sifat-sifat ikatan kimia dalam molekul.
3. J. A. Pople
J. A. Pople, seorang kimiawan teoretis Inggris-Amerika, mengembangkan metode perhitungan untuk mengestimasi elektronegativitas secara teoritis.
Metode yang dikembangkannya, yang dikenal sebagai metode perhitungan kuantum, membantu para ilmuwan dalam menghitung sifat-sifat elektronik unsur-unsur kimia, termasuk elektronegativitas.
4. Sanderson
Sanderson adalah seorang kimiawan Inggris yang mengusulkan konsep elektronegativitas berdasarkan karakteristik fisik dan kimia dari unsur-unsur.
Pendekatannya mencakup memperhitungkan volume atom, densitas muatan elektronik, dan sifat-sifat lainnya untuk memperkirakan elektronegativitas unsur-unsur kimia.
Secara umum, pengertian elektronegativitas menurut para ahli ini mengacu pada kemampuan suatu atom untuk menarik elektron dalam ikatan kimia.
Konsep ini merupakan alat penting dalam memahami sifat-sifat kimia unsur-unsur dan ikatan kimia antara unsur-unsur tersebut.
Melalui penggunaan skala elektronegativitas, para ilmuwan dapat memprediksi sifat-sifat ikatan kimia dan reaktivitas unsur-unsur dalam berbagai senyawa kimia.
Skala Elektronegativitas
Skala elektronegativitas adalah sebuah skala yang digunakan dalam kimia untuk mengukur relatif kemampuan suatu unsur kimia untuk menarik elektron dalam ikatan kimia.
Skala ini pertama kali diperkenalkan oleh Linus Pauling pada tahun 1932 dan telah menjadi alat penting dalam memahami sifat-sifat kimia unsur-unsur dan reaktivitas kimia mereka.
Berikut adalah penjelasan mengenai skala elektronegativitas:
1. Konsep dasar
Skala elektronegativitas didasarkan pada konsep bahwa dalam ikatan kimia antara dua atom, terdapat tarikan elektron yang tidak seimbang antara keduanya.
Atom yang memiliki elektronegativitas yang lebih tinggi akan menarik elektron lebih kuat daripada atom yang memiliki elektronegativitas yang lebih rendah.
2. Skala Pauling
Linus Pauling mengembangkan skala relatif untuk mengukur elektronegativitas unsur-unsur.
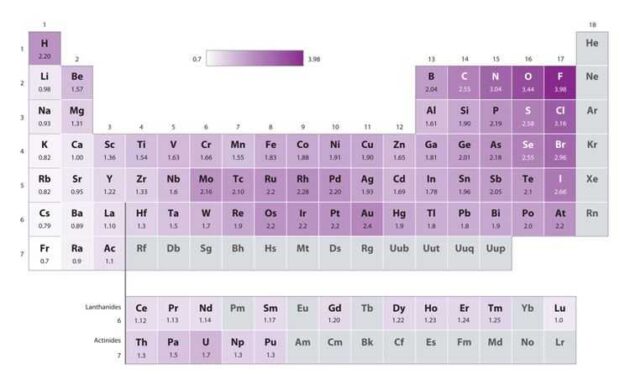
Pada skala Pauling, unsur fluor (F) memiliki nilai elektronegativitas tertinggi yaitu 4,0, sedangkan unsur-francium (Fr) memiliki nilai terendah dengan 0,7.
Sementara itu, unsur-unsur lainnya ditempatkan di antara kedua nilai ini berdasarkan perbandingan kemampuan mereka dalam menarik elektron.
3. Aplikasi dalam ikatan kimia
Skala elektronegativitas digunakan untuk memprediksi sifat-sifat ikatan kimia antara unsur-unsur. Dalam ikatan kovalen, perbedaan elektronegativitas antara dua atom menentukan polaritas ikatan tersebut.
Jika perbedaan elektronegativitas antara dua atom adalah nol, maka ikatan tersebut akan bersifat nonpolar. Namun, jika perbedaan tersebut signifikan, maka ikatan tersebut akan bersifat polar atau bahkan ionik.
4. Periode dan golongan dalam tabel periodik
Skala elektronegativitas juga memberikan wawasan tentang tren periodik dan tren golongan dalam tabel periodik.
Secara umum, elektronegativitas cenderung meningkat dari kiri ke kanan dalam suatu periode dan menurun dari atas ke bawah dalam suatu golongan.
Hal ini menunjukkan bahwa unsur-unsur di ujung kanan atas tabel periodik cenderung memiliki elektronegativitas yang tinggi, sementara unsur-unsur di ujung kiri bawah cenderung memiliki elektronegativitas yang rendah.
5. Keterbatasan
Meskipun skala Pauling telah banyak digunakan dalam studi kimia, terdapat beberapa kritik terhadap skala tersebut.
Beberapa peneliti berpendapat bahwa skala elektronegativitas Pauling tidak selalu konsisten dengan sifat-sifat ikatan kimia yang sebenarnya,
terutama ketika melibatkan unsur-unsur dengan perbedaan elektronegativitas yang kecil.
Dengan demikian, skala elektronegativitas merupakan konsep penting dalam kimia modern yang membantu dalam memahami sifat-sifat ikatan kimia dan reaktivitas unsur-unsur.
Meskipun memiliki keterbatasan, skala ini tetap menjadi alat yang berharga dalam analisis dan prediksi sifat-sifat kimia unsur-unsur.
Pentingnya Elektronegativitas dalam Ikatan Kimia
Elektronegativitas merupakan konsep yang sangat penting dalam kimia, terutama dalam memahami ikatan kimia antara atom-atom dalam suatu senyawa.
Elektronegativitas memengaruhi sifat-sifat ikatan kimia, polaritas senyawa, serta reaktivitas kimia unsur-unsur. Berikut adalah penjelasan rinci mengenai pentingnya konsep elektronegativitas dalam ikatan kimia:
1. Penentu Sifat Ikatan Kimia
Elektronegativitas merupakan faktor penentu utama dari sifat ikatan kimia.
Dalam ikatan kovalen, perbedaan elektronegativitas antara atom-atom yang terlibat menentukan apakah ikatan tersebut bersifat nonpolar, polar, atau bahkan ionik.
Semakin besar perbedaan elektronegativitas antara atom-atom tersebut, semakin polar atau ionik ikatan tersebut.
2. Prediksi Sifat Senyawa
Pemahaman tentang elektronegativitas memungkinkan para ilmuwan untuk memprediksi sifat-sifat senyawa, seperti titik didih, titik leleh, dan kelarutan.
Senyawa dengan ikatan polar atau ionik cenderung memiliki titik didih dan titik leleh yang lebih tinggi daripada senyawa nonpolar.
Selain itu, pengetahuan tentang polaritas senyawa memungkinkan para ilmuwan untuk memahami interaksi antar-molekul dalam senyawa-senyawa tersebut.
3. Klasifikasi Ikatan Kimia
Konsep elektronegativitas memungkinkan para ilmuwan untuk mengklasifikasikan berbagai jenis ikatan kimia, seperti ikatan kovalen nonpolar, ikatan kovalen polar, dan ikatan ionik.
Pemahaman yang baik tentang jenis ikatan ini sangat penting dalam memahami sifat-sifat senyawa dan reaktivitas kimia mereka.
4. Reaktivitas Unsur-unsur
Elektronegativitas juga memainkan peran penting dalam memahami reaktivitas kimia unsur-unsur.
Unsur-unsur dengan elektronegativitas yang tinggi cenderung menarik elektron dari unsur-unsur lain, sehingga cenderung berperilaku sebagai penerima elektron dalam reaksi kimia.
Sebaliknya, unsur-unsur dengan elektronegativitas yang rendah cenderung menjadi donor elektron.
5. Prediksi Polarisasi Ikatan
Dengan memahami elektronegativitas, para ilmuwan dapat memprediksi polarisasi ikatan dalam molekul-molekul kompleks.
Polarisasi ikatan ini memengaruhi sifat-sifat senyawa dan dapat digunakan dalam berbagai aplikasi,
termasuk dalam pemahaman tentang sifat-sifat senyawa polar dan nonpolar dalam berbagai bidang ilmu, seperti kimia organik dan kimia anorganik.
Pemahaman yang mendalam tentang konsep elektronegativitas secara signifikan memperkaya pemahaman kita tentang kimia, ikatan kimia, dan reaktivitas unsur-unsur.
Melalui penggunaan konsep ini, para ilmuwan dapat memprediksi dan menjelaskan berbagai fenomena kimia, serta merancang senyawa-senyawa dengan sifat-sifat yang diinginkan untuk berbagai aplikasi industri dan ilmiah.
Metode Penentuan Nilai Elektronegativitas
Terdapat beberapa metode yang digunakan untuk menentukan nilai elektronegativitas dari unsur-unsur kimia.
Beberapa metode ini didasarkan pada data eksperimental, sementara yang lain dikembangkan melalui analisis teoritis. Berikut adalah beberapa metode utama yang digunakan untuk menentukan nilai elektronegativitas:
1. Metode Skala Pauling
Metode ini dikembangkan oleh Linus Pauling dan merupakan salah satu metode paling umum yang digunakan untuk menentukan nilai elektronegativitas.
Dalam skala Pauling, unsur fluor (F) dianggap memiliki nilai elektronegativitas tertinggi yaitu 4,0. Nilai elektronegativitas unsur-unsur lain kemudian ditentukan relatif terhadap fluor.
2. Metode Berdasarkan Ikatan Senyawa
Metode ini melibatkan pengamatan sifat ikatan dalam senyawa kimia untuk menentukan perbedaan elektronegativitas antara unsur-unsur.
Contohnya adalah penentuan perbedaan elektronegativitas dalam ikatan kovalen polar dan ikatan ionik berdasarkan sifat-sifat fisik dan kimia senyawa tersebut.
3. Metode Berbasis Data Eksperimental
Metode ini melibatkan pengumpulan data eksperimental yang berkaitan dengan sifat-sifat fisik dan kimia unsur-unsur.
Data ini kemudian dianalisis untuk menentukan hubungan antara sifat-sifat ini dengan kemampuan unsur dalam menarik elektron.
Metode ini melibatkan teknik spektroskopi dan pengukuran lainnya untuk mengumpulkan data yang akurat.
4. Metode Perhitungan Kuantum
Metode ini melibatkan perhitungan teoritis yang kompleks berdasarkan prinsip-prinsip mekanika kuantum. Metode ini memanfaatkan model matematika untuk menghitung distribusi dan pergerakan elektron dalam atom.
Metode ini dapat menghasilkan nilai elektronegativitas yang mendekati nilai yang diperoleh dari data eksperimental.
5. Metode Berbasis Sifat Kimia dan Fisik
Beberapa ahli kimia menggunakan sifat-sifat kimia dan fisik dari unsur-unsur untuk menentukan nilai elektronegativitas.
Pendekatan ini melibatkan pengamatan tentang kemampuan unsur-unsur untuk menarik atau melepaskan elektron dalam reaksi kimia dan interaksi dengan unsur lain.
Setiap metode memiliki kelebihan dan keterbatasan sendiri, dan seringkali kombinasi dari beberapa metode ini diperlukan untuk mendapatkan nilai elektronegativitas yang akurat.
Pengembangan teknik-teknik baru dalam kimia dan ilmu terkait terus meningkatkan ketepatan dan keakuratan metode penentuan nilai elektronegativitas.
Hubungan Elektronegativitas dengan Sifat Molekul
Elektronegativitas memiliki hubungan yang erat dengan sifat molekul, terutama terkait dengan polaritas molekul dan reaktivitas kimia.
Elektronegativitas suatu atom dalam suatu molekul dapat mempengaruhi bagaimana elektron terdistribusi dalam molekul tersebut, yang pada gilirannya memengaruhi polaritas molekul dan reaktivitasnya terhadap senyawa lain.
Berikut adalah hubungan antara elektronegativitas dengan sifat molekul:
1. Polaritas Molekul
Perbedaan elektronegativitas antara atom-atom dalam suatu molekul menentukan sejauh mana elektron terdistribusi secara merata dalam molekul tersebut.
Jika perbedaan elektronegativitas antara atom-atom dalam molekul tersebut besar, molekul tersebut cenderung menjadi polar, dengan bagian yang lebih elektropositif dan bagian yang lebih elektronegatif.
Sebaliknya, jika perbedaan elektronegativitas antara atom-atom tersebut kecil, molekul tersebut cenderung menjadi nonpolar.
2. Kelarutan dalam Pelarut Polar dan Nonpolar
Elektronegativitas memengaruhi kelarutan suatu senyawa dalam pelarut polar atau nonpolar. Senyawa polar cenderung larut dalam pelarut polar, sedangkan senyawa nonpolar cenderung larut dalam pelarut nonpolar.
Hal ini terjadi karena senyawa polar dapat berinteraksi melalui gaya antarmolekul seperti ikatan hidrogen atau gaya van der Waals,
sedangkan senyawa nonpolar cenderung mengalami interaksi dengan pelarut nonpolar melalui gaya van der Waals.
3. Reaktivitas Kimia
Perbedaan elektronegativitas antara atom-atom dalam suatu molekul juga memengaruhi reaktivitas kimia molekul tersebut.
Molekul-molekul yang polar cenderung memiliki reaktivitas yang lebih tinggi karena bagian yang lebih elektropositif cenderung menarik elektron dari molekul lain,
sementara bagian yang lebih elektronegatif cenderung mendonasikan elektron.
Selain itu, molekul-molekul polar dapat berinteraksi dengan molekul lain melalui gaya antarmolekul yang lebih kuat.
4. Titik Didih dan Titik Leleh
Molekul-molekul polar cenderung memiliki titik didih dan titik leleh yang lebih tinggi dibandingkan dengan molekul nonpolar.
Hal ini terjadi karena gaya antarmolekul yang lebih kuat pada molekul polar, seperti ikatan hidrogen, yang membutuhkan energi lebih tinggi untuk memutus ikatan-ikatan tersebut.
5. Interaksi antarmolekul
Elektronegativitas memengaruhi interaksi antarmolekul dalam senyawa, termasuk interaksi antar-molekul polar-polar, polar-nonpolar, dan nonpolar-nonpolar.
Interaksi ini memainkan peran penting dalam memengaruhi sifat fisik dan kimia dari senyawa, seperti kelarutan, viskositas, tensi permukaan, dan sifat-sifat koligatif.
Dengan demikian, pemahaman tentang elektronegativitas memberikan wawasan yang dalam tentang sifat-sifat molekul dan bagaimana mereka berinteraksi dengan lingkungan sekitarnya.
Hal ini penting dalam memahami berbagai fenomena kimia dan fisik di alam serta dalam pengembangan berbagai aplikasi industri dan ilmiah.
Contoh Aplikasi Elektronegativitas dalam Kehidupan Sehari-hari
Elektronegativitas memiliki beragam aplikasi dalam kehidupan sehari-hari yang luas, mulai dari kimia dan industri, hingga bidang-bidang lain seperti kesehatan dan lingkungan.
Berikut adalah beberapa contoh aplikasi penting dari konsep elektronegativitas dalam kehidupan sehari-hari:
1. Aplikasi dalam Industri Kimia
Elektronegativitas digunakan dalam industri kimia untuk merancang senyawa-senyawa dengan sifat-sifat tertentu.
Misalnya, dalam industri farmasi, pemahaman tentang elektronegativitas memainkan peran penting dalam pengembangan obat-obatan dengan sifat-sifat reaktif yang diinginkan terhadap jaringan tertentu dalam tubuh.
2. Aplikasi dalam Elektronik dan Teknologi
Elektronegativitas penting dalam desain dan pembuatan berbagai perangkat elektronik seperti transistor, diode, dan berbagai sirkuit terintegrasi.
Pemahaman tentang perbedaan elektronegativitas membantu para insinyur dalam memilih bahan yang sesuai untuk komponen-komponen ini guna memastikan kestabilan dan efisiensi perangkat tersebut.
3. Aplikasi dalam Lingkungan Hidup
Elektronegativitas memainkan peran penting dalam memahami interaksi antara senyawa kimia dalam lingkungan hidup.
Misalnya, dalam pemrosesan limbah kimia, pemahaman tentang sifat-sifat polaritas dan kelarutan senyawa-senyawa kimia memungkinkan pengembangan metode pemrosesan yang lebih efisien dan ramah lingkungan.
4. Aplikasi dalam Ilmu Kesehatan
Pemahaman tentang elektronegativitas digunakan dalam berbagai penelitian ilmiah dalam bidang kedokteran, terutama dalam pemahaman tentang interaksi antara senyawa-senyawa obat dan jaringan biologis.
Hal ini penting dalam pengembangan obat-obatan yang memiliki target spesifik dalam tubuh manusia.
5. Aplikasi dalam Proses Pembersihan Air
Elektronegativitas digunakan dalam proses pembersihan air untuk menghilangkan kontaminan-kontaminan tertentu dari air limbah.
Proses seperti koagulasi dan flokulasi dalam pengolahan air bergantung pada interaksi antara molekul-molekul berbeda dengan memanfaatkan sifat polaritas dan nonpolaritasnya.
Aplikasi dalam Industri Bahan Bakar dan Energi: Elektronegativitas digunakan dalam penelitian dan pengembangan bahan bakar alternatif dan teknologi energi bersih.
Pemahaman tentang sifat-sifat polaritas molekul-molekul dalam bahan bakar membantu para ilmuwan dalam merancang bahan bakar yang lebih efisien dan ramah lingkungan.
Melalui aplikasi elektronegativitas dalam berbagai bidang kehidupan, kita dapat meningkatkan pemahaman kita tentang interaksi kimia di sekitar kita dan
mengembangkan solusi yang inovatif untuk berbagai tantangan di berbagai sektor kehidupan.
Dengan memanfaatkan konsep ini, kita dapat merancang dan mengembangkan berbagai produk dan teknologi yang memberikan dampak positif bagi kehidupan sehari-hari dan lingkungan.
Faktor-faktor yang Mempengaruhi Nilai Elektronegativitas
Nilai elektronegativitas suatu unsur dapat dipengaruhi oleh sejumlah faktor yang berbeda. Faktor-faktor ini mencakup struktur atom, jumlah proton, konfigurasi elektron, dan sifat-sifat kimia unsur tersebut.
Berikut adalah faktor utama yang memengaruhi nilai elektronegativitas:
1. Jumlah Proton dalam Inti Atom
Jumlah proton dalam inti atom memengaruhi nilai elektronegativitas karena proton memberikan muatan positif pada inti atom.
Semakin banyak proton dalam inti atom, semakin besar tarikan elektron ke inti atom tersebut, sehingga nilai elektronegativitasnya cenderung lebih tinggi.
2. Ukuran Atom
Ukuran atom juga memengaruhi nilai elektronegativitas.
Atom yang lebih kecil cenderung memiliki nilai elektronegativitas yang lebih tinggi karena elektron-elektron dalam kulit valensi berada lebih dekat dengan inti atom dan oleh karena itu, lebih tertarik ke inti atom.
3. Konfigurasi Elektron
Konfigurasi elektron suatu atom memainkan peran penting dalam menentukan nilai elektronegativitas.
Konfigurasi elektron menentukan sejauh mana kulit valensi atom tersebut terisi dan seberapa mudahnya atom tersebut menarik atau melepaskan elektron.
Atom dengan konfigurasi elektron yang mendekati konfigurasi gas mulia cenderung memiliki nilai elektronegativitas yang tinggi.
4. Elektron Afinitas
Elektron afinitas adalah energi yang dilepaskan atau diserap ketika suatu atom menangkap satu elektron tambahan.
Atom dengan elektron afinitas yang tinggi cenderung memiliki nilai elektronegativitas yang tinggi karena mereka cenderung menarik elektron tambahan dengan kuat.
5. Kekuatan dan Jarak Ikatan
Jarak dan kekuatan ikatan antara atom-atom dalam molekul atau senyawa juga dapat memengaruhi nilai elektronegativitas.
Ikatan yang lebih kuat antara atom-atom cenderung menunjukkan perbedaan elektronegativitas yang besar antara atom-atom tersebut, menghasilkan ikatan kovalen polar atau bahkan ikatan ionik.
Pemahaman yang mendalam tentang faktor-faktor yang memengaruhi nilai elektronegativitas ini memungkinkan
para ilmuwan untuk memahami sifat-sifat kimia unsur-unsur dan memprediksi interaksi kimia antara unsur-unsur tersebut.
Selain itu, hal ini juga memainkan peran penting dalam pengembangan berbagai aplikasi di berbagai bidang, mulai dari industri kimia hingga ilmu kesehatan dan teknologi energi.
Kesimpulan
Elektronegativitas merupakan konsep kunci dalam kimia yang menggambarkan kemampuan suatu atom untuk menarik pasangan elektron dalam suatu ikatan kimia.
Konsep ini memainkan peran penting dalam memahami sifat-sifat ikatan kimia, polaritas molekul, dan reaktivitas kimia unsur-unsur.
Melalui penggunaan skala elektronegativitas, para ilmuwan dapat memprediksi sifat-sifat ikatan kimia dan reaktivitas unsur-unsur dalam berbagai senyawa kimia.

Perkenalkan nama saya Rita Elfianis, Seorang tenaga pengajar di Universitas Islam Negeri Suska RIAU. Semoga artikel yang dibuat bermanfaat